Apesar do ferro (Fe) ser o quarto elemento mais abundante (5.1%) na litosfera, a deficiência de Fe é um dos problemas mais antigos e difíceis de controlar em plantas cultivadas em solos de origem calcária. Uma das razões prende-se com o facto de, nestas condições, a fração disponível (Fe solúvel) para as plantas ser muito inferior à de Fe total no solo, pois os sais férricos e ferrosos reagem rapidamente com o CaCO3 originando óxidos de Fe de baixa solubilidade e não acessíveis para as plantas. A este efeito acresce a presença do ião bicarbonato que, na planta, irá manter o pH apoplástico em valores que interferem com a atividade do grupo de certas enzimas, tal como as qQuelato de ferro redutases – QFR, essenciais no processo de absorção, transporte e distribuição do Fe no interior das plantas. A homéostase do Fe nas plantas, ou a manutenção dos níveis adequados de Fe na planta, é assegurada não só pelo percurso do Fe desde a raiz até às folhas, como pela distribuição e acumulação deste elemento na planta. Diversos compostos tem um papel preponderante neste processo como o ácido cítrico, a nicotianamina e a fitoferritina, proteína de reserva com Fe.
Genericamente, quando a maioria das árvores de fruto são instaladas em solos de origem calcária existem diversas barreiras bioquímicas que perturbam o longo percurso do Fe no continum solo-planta e induzem o aparecimento dos sintomas característicos da deficiência de Fe ou clorose férrica. A clorose férrica traduz-se pelo amarelecimento do limbo foliar com aspeto de um fino reticulado no qual apenas as nervuras permanecem verdes, surgindo inicialmente nas folhas mais jovens (Figura 1).

Figura 1 – Sintomas de deficiência de ferro ou clorose férrica (morangueiro, alfarrobeira, porta-enxerto de citrinos)
Como consequência, as árvores cloróticas apresentam decréscimos na produção total, quer pelo menor número de frutos produzidos, quer pela produção de frutos de menor calibre. Acresce que a composição interna dos frutos e a época de maturação, determinantes na data da colheita, também são afetadas. Sempre que uma fruteira apresenta clorose férrica estes impactos negativos prevalecem durante vários anos, pois as reservas nutritivas são afetadas e a produção também, reforçando a necessidade de corrigir esta deficiência. Habitualmente recorre-se à aplicação massiva de quelatos sintéticos, ao solo e/ou foliar, mas que devido aos custos e às questões ambientais tem desencadeado a procura de alternativas, como a de novos agentes complexantes derivados de produtos naturais, como sejam lignosulfonatos, humatos, citratos, gluconatos, aminoácidos, entre outros. Atualmente, a bem do ambiente, procuram-se quelatos (complexos) menos estáveis para o Fe, mas biodegradáveis e mais seletivos, para evitar que após a absorção do Fe, os agentes complexantes permaneçam no ambiente com oportunidade de quelatar outros elementos metálicos, nomeadamente metais pesados, contaminando a cadeia trófica. Nos últimos anos têm vindo a ser propostas alternativas que promovam o uso das reservas internas de Fe ou que ultrapassem as barreiras bioquímicas já mencionadas, nomeadamente ao nível da interação com o microbioma da rizosfera, usando compostos complexantes libertados pelos microrganismos, os sideróferos, que têm elevada afinidade para o Fe. A associação de práticas de fertilização química com a colonização biológica da rizosfera pode otimizar o uso do Fe e diminuir impactos ambientais. Outra vertente decorre de haver grupos de plantas, que quando em stress, libertam complexantes do Fe para a rizosfera à semelhança dos microrganismos, denominados por fitosideróferos (FS).
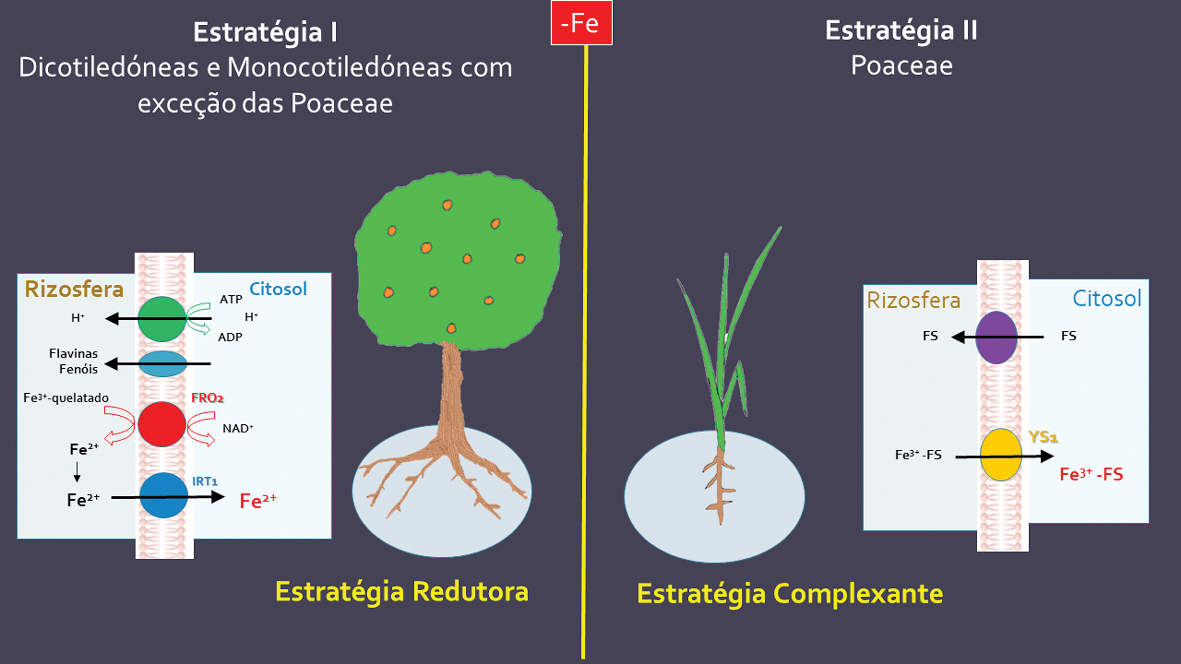
Figura 2 – Esquema das estratégias de utilização do ferro. FS – fitosideróferos
As plantas quando sujeitas à deficiência de Fe podem ser reunidas em dois grupos (Figura 2): i) Estratégia I ou estratégia redutora, presente na maior parte das espécies agrícolas, em que se verifica o aumento da atividade da QFR e a excreção de compostos fenólicos a nível radicular na tentativa de acidificação do meio circundante mas sem efeito em solos de origem calcária; e ii) Estratégia II ou complexante, a qual inclui as plantas que pertencem à família das Poacea (gramíneas), e se caracterizam por segregar para a rizosfera os mencionados agentes complexantes do Fe (FS), muito estáveis e com elevada afinidade para o Fe mesmo em meios alcalinos, como sejam os solos de origem calcária.
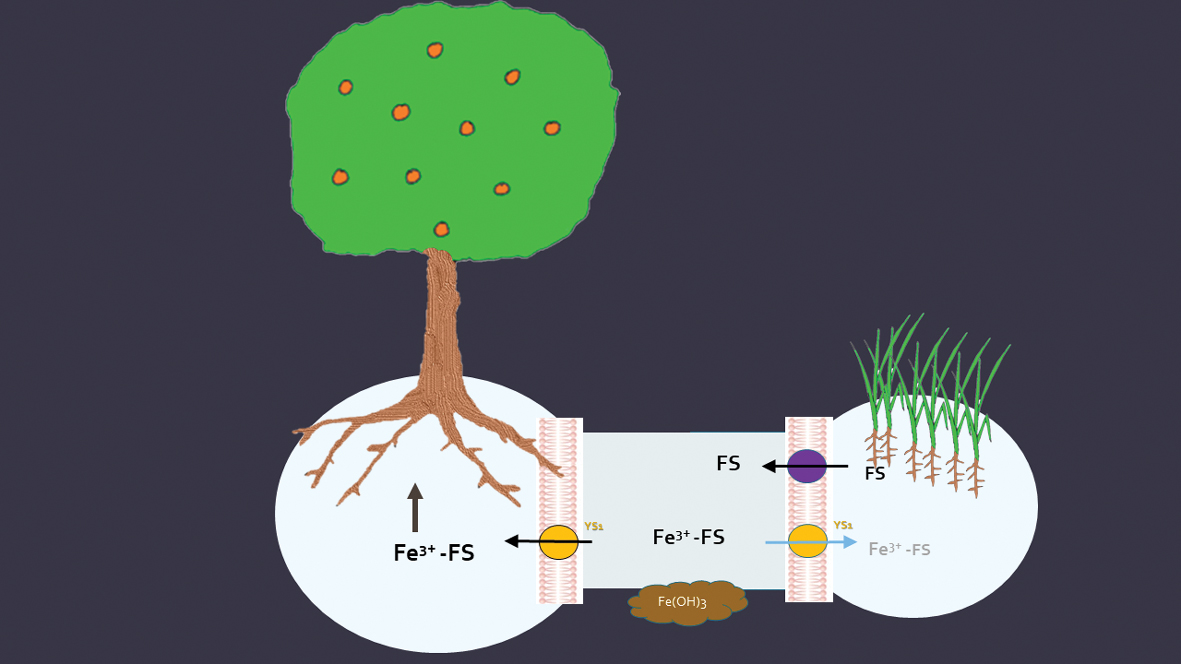
Figura 3 – Sinergia resultante da partilha da rizosfera por espécies com estratégias diferentes
Quando as duas estratégias se encontram, espacial e temporalmente, é possível identificar um sinergismo, isto é, as plantas da Estratégia II (gramíneas) poderão libertar agentes complexantes para a rizosfera partilhada, que irão complexar o Fe existente, protegendo-o das consequências da reação alcalina e permitindo a sua entrada nas plantas da Estratégia I, como as árvores de fruto (Figura 3). É a abordagem da consociação, neste caso pensada especificamente para a deficiência de Fe e que consiste na sementeira de espécies da estratégia II nas entrelinhas dos pomares de fruteiras. É um procedimento complementar que não elimina o recurso à fertilização de Fe, mas reduz a quantidade e o número de aplicações de quelatos de Fe.
Como os complexantes do Fe produzidos pelas gramíneas estão na parte aérea é possível recorrer a extratos vegetais preparados a partir da maceração destas espécies, como foi testado na Universidade do Algarve (Patente Nacional nº 103584 de 13 de julho 2009) pela aplicação foliar. Esta é uma alternativa de gestão sustentável da fertilização do Fe em hortícolas. Resumindo, atualmente, procuram-se abordagens que nos permitam tirar partido da natureza, minimizando as intervenções e assegurando a produtividade essencial à crescente demanda de produtos mais saudáveis.
Indubitavelmente que nos últimos anos houve um grande avanço sobre o estudo da clorose férrica induzida em solos calcários. No entanto, muitos aspetos permanecem por conhecer em especial aqueles que têm a ver com as condições de crescimento em campo, os mecanismos de resposta e o grau de tolerância das diferentes espécies vegetais. Futuramente, o estudo da clorose férrica deverá ir além da produção, da economia e do ambiente, pois parece haver repercussões ainda não identificadas a nível social e de saúde humana.
Um artigo de Maribela Pestana & Pedro José Correia
MeditBio, Universidade do Algarve, Faculdade de Ciências e Tecnologia, Campus de Gambelas 8005-139 Faro
Publicado na Voz do Campo n.º 228 (julho 2019)